血管性头痛是困扰全球数亿人的常见疾病,其典型表现为单侧或双侧搏动性疼痛,常伴随恶心、畏光、畏声等症状。据最新统计,中国约有1.3亿偏头痛患者,但仅有约半数患者主动就医,其中超过80%存在治疗不规范或药物滥用等问题。本文将结合最新科研成果,系统解析血管性头痛的发病机制、治疗药物创新及临床应用策略。
一、血管性头痛的病理机制突破
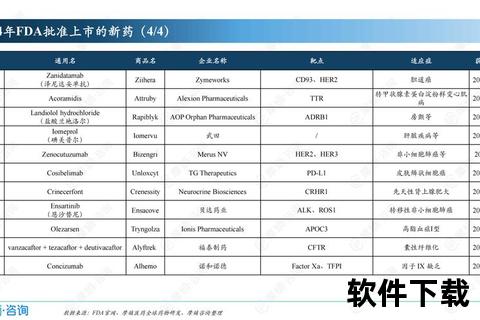
传统理论认为血管异常收缩扩张是核心诱因,但近年研究发现三叉神经-血管系统的神经源性炎症才是关键驱动因素。当三叉神经末梢释放降钙素基因相关肽(CGRP)、垂体腺苷酸环化酶激活肽(PACAP)等神经肽时,会引发脑膜血管扩张和炎症反应,形成疼痛信号传递至中枢。
新机制发现:2024年《科学》杂志报道的脑脊液流动假说揭示了另一条通路——脑脊液携带CGRP等分子直接浸润三叉神经节基底池,激活神经元引发头痛。这一发现为开发非CGRP靶点药物提供了新方向。
二、治疗药物发展历程与创新靶点
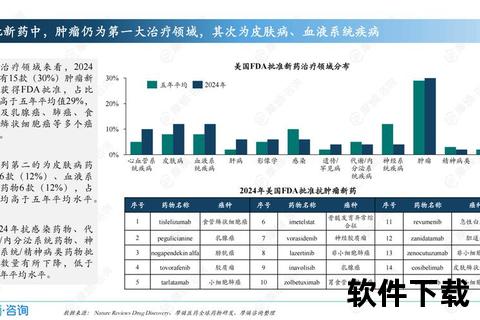
1. 传统药物局限性分析
早期治疗依赖非甾体抗炎药(布洛芬)、曲普坦类药物,但存在三大缺陷:
2. CGRP靶向药物革命
作为近十年最重要的突破,CGRP靶向药物分为两类:
代表药物:Erenumab(Aimovig)、Fremanezumab(Ajovy)
优势:生物利用度高,预防效果显著(减少头痛天数50%以上)
缺点:需注射给药,起效较慢(2-4周)
代表药物:Rimegepant(Nurtec)、Zavegepant(Zavzpret)
突破性:15分钟起效,兼具急性治疗与预防功能
临床数据:使用Rimegepant后48小时无痛率达21.2%,复发率降低至42%
特殊人群应用:CGRP药物因不通过肝代谢、无心血管风险,成为妊娠期(需医生评估)、高血压患者的优选方案。
3. 下一代靶点:PACAP信号通路
2024年《新英格兰医学杂志》披露的Lu AG09222是全球首个靶向PACAP的单抗,III期试验显示34%患者头痛天数减少≥50%,且对CGRP药物无效者仍可获益。该靶点可能改写难治性偏头痛治疗格局。
三、临床用药决策树与注意事项
1. 个体化用药选择建议(见图1)
[此处建议插入用药决策流程图,包含以下判断节点]
2. 避免药物滥用的三大原则
1. 急性药物:每月使用≤10天,NSAIDs与曲普坦类交替使用
2. 预防药物:CGRP单抗应持续使用≥3个月评估疗效
3. 监测指标:肝肾功能(小分子药物)、注射部位反应(单抗)
四、家庭管理与就医信号
1. 急性发作期处理步骤
1. 环境调整:静卧于黑暗安静环境,冷敷前额
2. 药物干预:确诊患者立即服用Rimegepant口崩片(无需饮水)
3. 症状监测:记录头痛持续时间、伴随症状(视力异常需警惕卒中)
2. 必须就医的预警信号
五、未来治疗展望
2025年值得关注的三大趋势:
1. 双靶点药物:辉瑞研发中的CGRP+PACAP双抗已进入II期临床
2. 基因疗法:针对家族性偏瘫型偏头痛的基因编辑试验启动
3. 穿戴设备:经皮电刺激仪(Nerivio)获FDA批准,通过调节CGRP释放实现无药缓解
血管性头痛治疗已从"止痛"迈向"治本"时代。建议患者建立头痛日记,在神经内科医生指导下制定阶梯式治疗方案。对于每月发作超过4次、严重影响生活质量者,应尽早启动CGRP靶向药物预防,避免病程慢性化。医疗从业者需注意,2025年中国自主研发的BR005等新型药物进入II期临床,将为患者提供更多选择。
